Das schafft einen interessanten Ausgangspunkt: Denn zwischen der privaten Nutzung – geprägt von persönlichem Orientierungsbedarf und einer direkten User Experience – und dem professionellen Einsatz im Versorgungsalltag liegen nicht nur unterschiedliche Anforderungen, sondern auch sehr unterschiedliche Vorstellungen davon, was KI leisten soll und darf.
Entwicklung und Spannungsfeld
Die Interpretation medizinischer Daten erfolgt im Gesundheitswesen auf mehreren Ebenen – von der Messung einzelner Laborwerte bis zur komplexen Therapieentscheidung. Mit der rasanten Entwicklung großer Sprachmodelle (LLMs) wie ChatGPT Health und Claude for Healthcare entstehen neue Werkzeuge, die eine hochgradig aggregierte Interpretation ermöglichen. Das schafft ein Spannungsfeld: Einerseits bieten LLMs eine ganzheitliche Sicht auf verstreute Gesundheitsdaten und liefern Nutzer:innen direkt verwertbare Einordnungen. Andererseits stehen sie im Vergleich zur traditionellen, spezialisierten Interpretation durch medizinische Fachkräfte – insbesondere dort, wo kontextabhängige, regelbasierte und fachlich tiefe Befundung nötig ist.
Dieser Beitrag beleuchtet die Ebenen der Dateninterpretation, die reale Nutzung von LLMs im Gesundheitswesen (trotz verständlicher Vorbehalte) und warum eine differenzierte, mehrstufige Interpretation – gerade in der Labormedizin – weiterhin unverzichtbar bleibt.
Wie wir Nutzung verstehen: Befragung versus reales Verhalten
Die Diskussion um LLMs in der Medizin wird oft von berechtigten Vorbehalten begleitet: Datenschutz, Verantwortlichkeiten, fehlende Transparenz, potenzielle Halluzinationen und die Frage, ob sensible Informationen in Online-Systeme gehören.
Gleichzeitig zeigt sich in der Praxis eine dynamische Realität: Viele nutzen GPT & Co. bereits – teils offiziell in Pilotkontexten, teils informell als „zweites Paar Augen“ für Formulierungen, Zusammenfassungen oder Einordnungen.
Methodisch lässt sich das in zwei Perspektiven fassen:
- Befragungen: Was geben Ärzt:innen, wie sie KI nutzen (oder nutzen würden)?
- Reales Verhalten: Was wird tatsächlich genutzt, in welchen Situationen und mit welchen Mustern?
Gerade diese zweite Perspektive ist oft aufschlussreich, weil sie zeigt, wo der klinische Alltag heute bereits pragmatisch Entscheidungen trifft – unabhängig davon, ob die Debatte vollständig geklärt ist.
LLMs im Gesundheitswesen: neue Werkzeuge, neue Nutzungskontexte
Große Sprachmodelle haben in kurzer Zeit Einzug in den Gesundheitsbereich gehalten. Dabei lassen sich zwei unterschiedliche Stoßrichtungen beobachten:
- Endnutzer:innen-orientierte Anwendungen (z. B. ChatGPT Health)
Diese Systeme sind darauf ausgelegt, Menschen beim Verstehen ihrer Gesundheitsinformationen zu unterstützen: Erklärungen zu Befunden, Vorbereitung auf Arztgespräche, Zusammenfassungen und Trendbetrachtungen. Der Fokus liegt häufig auf Verständlichkeit, Orientierung und der Verbindung verschiedener persönlicher Datenquellen. - Professionelle bzw. B2B-orientierte Anwendungen (z. B. Claude for Healthcare)
Hier steht die Einbettung in Prozesse von Leistungserbringern und Kostenträgern im Vordergrund: Dokumentationsunterstützung, administrative Workflows, strukturierte Aufbereitung von Informationen, sowie die datenschutzkonforme Integration in bestehende Systeme.
Wichtig ist: Beide Richtungen verschieben Interpretation nach „oben“ – weg von einzelnen Datenpunkten hin zu aggregierten, fallbezogenen Zusammenfassungen. Das ist sinnvoll, birgt aber auch Risiken, wenn Spezifität, Referenzlogik, lokale Standards und diagnostische Pfade nicht sauber berücksichtigt werden.
Der Datenstack: Von der Generierung bis zur Therapieentscheidung
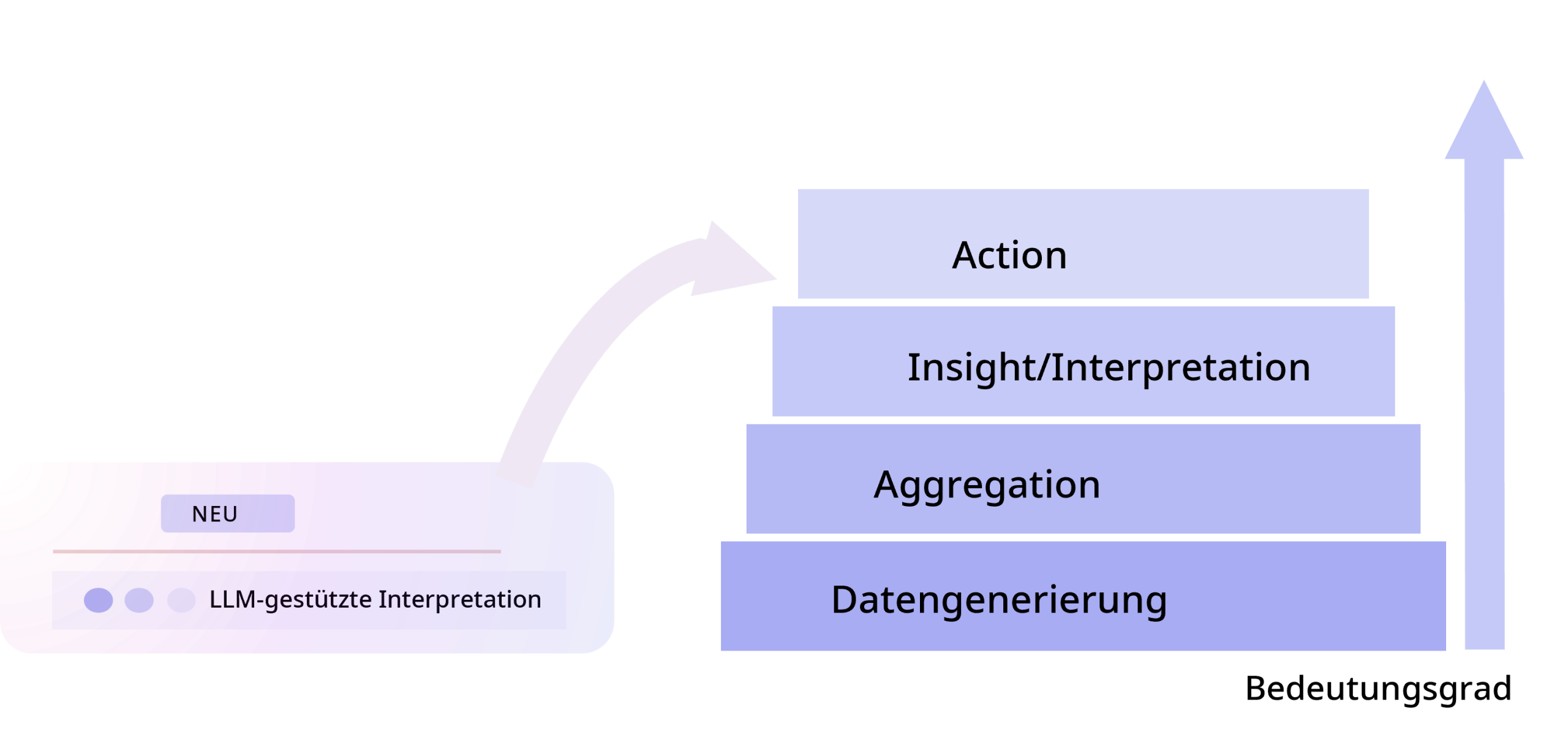
Um zu verstehen, auf welcher Ebene interpretierende Systeme wirken, hilft ein Blick auf den „Datenstack“ im Gesundheitswesen:
Grundsätzlich gilt: Je weiter oben im Stack interpretiert wird, desto mehr Informationen stehen potenziell zur Verfügung – etwa wenn neben Laborwerten auch Radiologie, Klinikverlauf und Medikation einfließen. Gleichzeitig steigt die Gefahr, dass spezifische diagnostische Logik „verallgemeinert“ wird und lokale Details untergehen.
Das Labor als Ort klinischer Interpretation
Laboratorien werden oft als Datenlieferanten gesehen – faktisch sind sie jedoch auch Orte hochspezialisierter Interpretation. Labormedizin bedeutet nicht nur Messung, sondern auch:
- technische Validierung (Analytik, Plausibilität, Präanalytik)
- kontextualisierte Einordnung (Referenzintervalle, Interferenzen, Muster)
- Kommunikation und Beratung entlang klinischer Fragestellungen
- strukturierte Befundkommentare und Hinweise zur Einordnung
Gerade in komplexen Fragestellungen ist „Interpretation im Labor“ ein wichtiger Bestandteil der diagnostischen Qualität.
Reflex und „Insight to Action“: warum Workflows entscheidend sind
Ein zentraler Mehrwert entsteht nicht allein durch „bessere Texte“, sondern durch intelligente Workflows, die Interpretation in Handlung übersetzen – und zwar regelbasiert, nachvollziehbar und reproduzierbar.
Das Prinzip lässt sich so beschreiben:
- Insight: Erkennen, was der Befund in diesem Kontext bedeutet (inkl. Unsicherheiten und Alternativen).
- Action: ableiten, was sinnvollerweise als nächster Schritt erfolgen sollte (z. B. Zusatzparameter, Verlaufskontrolle, Differenzierungstest).
Gerade in der Labormedizin ist dieses „Insight to Action“ seit Jahren etabliert – etwa über definierte Diagnostikpfade und Reflexstrategien. LLMs können hier ergänzen, indem sie Informationen verständlich bündeln oder klinische Kontexte strukturieren. Der entscheidende Unterschied bleibt jedoch: Workflows müssen lokal korrekt sein (Referenzen, SOPs, Indikationslogik, Verantwortlichkeiten) und dürfen nicht durch generische, global gemittelte Antworten ersetzt werden.
Praxisbeispiele: Wo Spezialwissen gefragt ist
Es gibt diagnostische Bereiche, in denen domänenspezifische Tiefe entscheidend ist und generische, hochaggregierte Interpretation typischerweise an Grenzen stößt – insbesondere dann, wenn Referenzlogik, Spezialmethodik oder kontextabhängige Algorithmen erforderlich sind:
Liquordiagnostik (Reiber-Schema und oligoklonale Banden)
Hier reichen „Laborwerte erklären“ und allgemeine Aussagen selten aus. Die diagnostische Aussage entsteht aus Mustern, Relationen (Serum/Liquor), methodischen Besonderheiten und dem Zusammenspiel der Parameter.
Spezielle Gerinnungsdiagnostik
Die Interpretation hängt oft an Konstellationen, Mischversuchen, klinischem Kontext (z. B. Antikoagulation) und klaren Pfaden zur Abklärung von Mangel versus Inhibitor. Das ist regelbasiert – aber nicht trivial.
Therapeutisches Drug Monitoring (TDM)
Spiegelwerte sind ohne Zeitbezug, Dosierung, Interaktionen und klinische Zielbereiche nur eingeschränkt interpretierbar. Besonders wichtig ist die Differenzierung zwischen „auffällig“ und „handlungsrelevant“.
Genetik und Mikrobiom (als Beispiele für hochkomplexe Domänen)
Hier entstehen Interpretationen aus Datenpipelines, Klassifikationslogik und Fachstandards. Die Herausforderung ist weniger „Wissen“, sondern die korrekte Einordnung unter definierten Regeln.
Der gemeinsame Nenner: Je spezialisierter die Fragestellung, desto stärker wird die Diagnostik zu einer Kombination aus Daten, Regeln, Kontext und Erfahrung. Genau hier bleibt Befundung auf Labor- bzw. Fachebene eine eigene, nicht substituierbare Wertschöpfung – analog zu spezialisierter KI in der Radiologie, die nicht „alles“ kann, aber in einem klaren Bereich sehr präzise ist.
Fazit: Warum differenzierte Interpretation auf mehreren Ebenen notwendig bleibt
Große KI-Sprachmodelle eröffnen neue Horizonte in der medizinischen Informationsverarbeitung. Sie können riesige Datenmengen schnell bündeln, Zusammenfassungen erstellen und Patient:innen wie auch Fachkräften eine breitere Perspektive auf komplexe Sachverhalte ermöglichen. Doch so beeindruckend diese Breite ist: Sie ersetzt nicht automatisch die diagnostische Tiefe, die in spezialisierten Ebenen des Systems entsteht – insbesondere dort, wo Referenzlogik, lokale Prozesse und Domänenwissen den Unterschied machen.
Die mehrstufige Interpretation – von der Validierung einzelner Messwerte bis zur ganzheitlichen Therapieempfehlung – bleibt auch im KI-Zeitalter notwendig. Jeder dieser Schritte fügt Wert hinzu: Die Laboranalyse stellt die verlässliche Datenbasis, die ärztliche Expertise im Fachgebiet sorgt für korrekte Deutung der einzelnen Puzzleteile, und die LLM-gestützte Aggregation kann daraus ein Gesamtbild formen und bei der Entscheidungsfindung helfen. Wird eine Ebene vernachlässzt, leidet das Gesamtergebnis. Nur durch Integration aller Ebenen kann gewährleistet werden, dass Patien:innen von sowohl umfassenden als auch präzisen Interpretationen profitieren. Die Zukunft der medizinischen Dateninterpretation liegt folglich in einem hybriden Ansatz: globale KI-Intelligenz einerseits, lokale medizinische Intelligenz andererseits – verknüpft durch intelligente Workflows zum Wohle besserer Diagnostik und Therapie.
Drei Learnings für die Labormedizin im KI-Zeitalter
- Domänen-Know-how bleibt ein Differenzierer – besonders in der Tiefe
Ein erheblicher Teil diagnostischer Wertschöpfung entsteht dort, wo Speziallogik zählt: oligoklonale Banden und Reiber-Schema, spezielle Gerinnung, TDM, Genetik/Mikrobiom. Diese Bereiche profitieren von KI, aber sie verlangen domänenspezifische Modelle, Regeln und Expertise – nicht nur allgemeine Textgenerierung. - Wer im Ökosystem relevant sein will, muss Daten bidirektional sauber gestalten
Die Qualität entsteht nicht durch „mehr Daten“, sondern durch strukturierte, konsistente und kontextualisierte Daten. Entscheidend ist zudem die Rückkopplung: Nur wenn relevante Kontextdaten (klinische Informationen, Vorbefunde, Therapieverlauf) zurückfließen, kann Interpretation an der richtigen Stelle präziser werden. - Intelligente Workflows verbinden Insight und Action
Der Hebel liegt in der Orchestrierung: Erkennen, was möglich und sinnvoll ist, und daraus den nächsten Schritt ableiten – idealerweise über klare, nachvollziehbare Pfade (inkl. Reflexstrategien und definierter Verantwortlichkeiten). LLMs können unterstützen, aber der Workflow muss fachlich sauber und lokal korrekt sein.